
مقدمه:
ساختار مولکولی و زاویههای پیوندی از مباحث اساسی در شیمی دهم هستند که به درک دقیقتر رفتار مولکولها کمک میکنند. این موضوعات در سوالات نهایی و کنکور بسیار پرتکرار هستند و تسلط بر آنها میتواند به شما در موفقیت در آزمونها کمک کند. در این مقاله، به بررسی انواع ساختارهای مولکولی، زاویههای پیوندی و عوامل تأثیرگذار بر این زاویهها میپردازیم و چهار شکل آموزشی برای فهم بهتر موضوع ارائه میدهیم. همچنین، نکات طلایی که در آزمونهای نهایی و کنکور اهمیت دارند را مرور خواهیم کرد.
ساختار مولکولی و نظریه VSEPR
ساختار مولکولی نشاندهنده نحوه قرارگیری اتمها در یک مولکول و زاویههای بین پیوندها است. برای پیشبینی شکل هندسی مولکولها، از نظریه دفع زوج الکترون لایه ظرفیت (VSEPR) استفاده میشود. این نظریه بر اساس دفع الکترونهای اطراف اتم مرکزی است و کمک میکند تا ساختار مولکول به گونهای باشد که انرژی کمینه شود.
انواع ساختارهای مولکولی
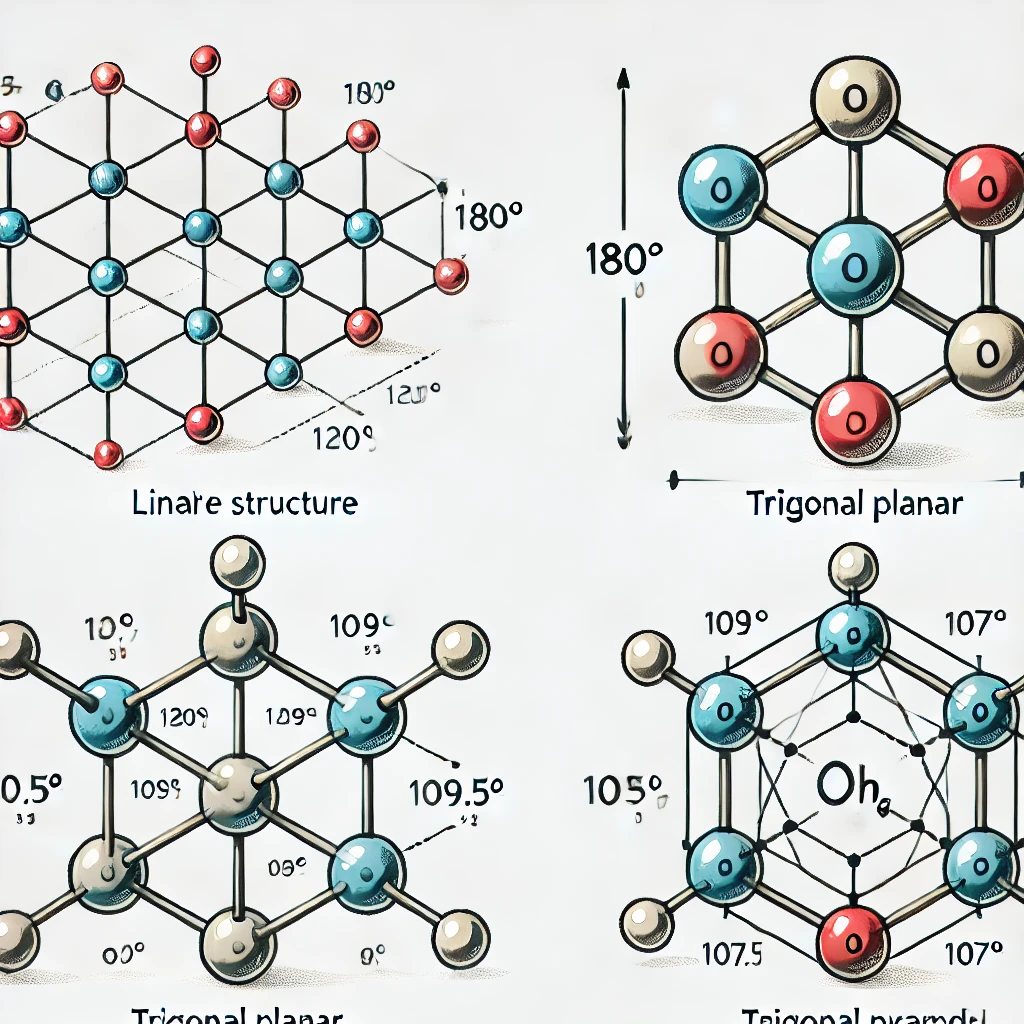
- ساختار خطی (Linear)
- ویژگیها: در این ساختار، اتمها به صورت خطی قرار میگیرند و زاویه پیوندی 180 درجه است.
- مثال: مولکول دیاکسید کربن (CO₂) یک نمونه از ساختار خطی است.
- شکل مرتبط: تصویر نشاندهنده یک مولکول خطی با زاویه 180 درجه.
2. ساختار مثلثی مسطح (Trigonal Planar)
- ویژگیها: در این ساختار، سه اتم در اطراف اتم مرکزی قرار دارند و زاویه پیوندی 120 درجه است.
- مثال: مولکول BF₃ دارای ساختار مثلثی مسطح است.
- شکل مرتبط: تصویر نشاندهنده یک مولکول مثلثی مسطح با زاویه 120 درجه.
3. ساختار چهاروجهی (Tetrahedral)
- ویژگیها: در این ساختار، چهار اتم به صورت متقارن در اطراف اتم مرکزی قرار دارند و زاویه پیوندی 109.5 درجه است.
- مثال: متان (CH₄) نمونهای از یک مولکول با ساختار چهاروجهی است.
- شکل مرتبط: تصویر نشاندهنده یک مولکول چهاروجهی با زاویه 109.5 درجه.
4. ساختار هرمی مثلثی (Trigonal Pyramidal)
- ویژگیها: در این ساختار، سه اتم و یک جفت الکترون تنها در اطراف اتم مرکزی قرار دارند. زاویه پیوندی کمی کمتر از 109.5 درجه است.
- مثال: آمونیاک (NH₃) دارای ساختار هرمی مثلثی است.
- شکل مرتبط: تصویر نشاندهنده یک مولکول هرمی مثلثی با زاویه حدود 107 درجه.
عوامل مؤثر بر زاویههای پیوندی
- زوجهای الکترونی غیرمشترک: وجود زوجهای الکترونی غیرمشترک در اطراف اتم مرکزی باعث میشود که زاویههای پیوندی کاهش یابند، زیرا این زوجها فضای بیشتری را اشغال میکنند و باعث دفع بیشتر میشوند. برای مثال، در آمونیاک (NH₃)، جفت الکترون غیرمشترک باعث کاهش زاویه پیوندی به حدود 107 درجه میشود.
- الکترونگاتیویته: اختلاف الکترونگاتیویته بین اتمها میتواند تأثیر مستقیمی بر زاویههای پیوندی داشته باشد. اتمهای با الکترونگاتیویته بالا، الکترونها را به سمت خود جذب کرده و ممکن است زاویه پیوندی را تغییر دهند.
- تعداد پیوندها: تعداد پیوندهای یگانه، دوگانه یا سهگانه بین اتمها نیز بر زاویههای پیوندی تأثیر دارد. پیوندهای دوگانه و سهگانه فضای بیشتری نسبت به پیوند یگانه اشغال میکنند و میتوانند زاویهها را تحت تأثیر قرار دهند.
نکات طلایی و پرتکرار برای کنکور و سوالات نهایی
- زاویه پیوندی چهاروجهی (109.5 درجه): زاویه پیوندی در ساختار چهاروجهی یکی از نکات پرتکرار در سوالات نهایی و کنکور است. به خاطر داشته باشید که در غیاب جفتهای الکترونی غیرمشترک، زاویه دقیقاً 109.5 درجه است.
- تأثیر جفتهای الکترونی تنها: جفتهای الکترونی غیرمشترک همیشه زاویه پیوندی را کاهش میدهند. برای مثال، در آمونیاک (NH₃) زاویه کمی کمتر از 109.5 درجه و در آب (H₂O) زاویه حدود 104.5 درجه است.
- تشخیص ساختار مولکولی با استفاده از VSEPR: یکی از سوالات پرتکرار کنکور، تشخیص شکل هندسی مولکول با استفاده از نظریه VSEPR است. این نظریه به شما کمک میکند تا به راحتی ساختار مولکول و زاویههای پیوندی را پیشبینی کنید.
جمعبندی
ساختار مولکولی و زاویههای پیوندی از مباحث پایهای و مهم در شیمی دهم هستند که در سوالات نهایی و کنکور به صورت پرتکرار مطرح میشوند. درک ساختارهای مختلف مانند خطی، مثلثی مسطح، چهاروجهی و هرمی مثلثی و تسلط بر نظریه VSEPR به شما کمک میکند تا به سوالات مربوطه با اطمینان پاسخ دهید. نکات طلایی این مقاله به شما کمک میکند تا در کنکور و امتحانات نهایی موفقتر عمل کنید.
پیشنهاد مطالعه بیشتر:
برای درک بهتر ساختارهای مولکولی و زاویههای پیوندی، مطالعه دقیق کتاب شیمی دهم و مشاهده ویدیوهای آموزشی مرتبط توصیه میشود. همچنین، تمرین سوالات پرتکرار کنکور و سوالات نهایی به تقویت تسلط شما بر این مبحث کمک میکند.