
عدد اکسایش یکی از مفاهیم اساسی در شیمی دوازدهم است که برای درک واکنشهای شیمیایی، بهویژه واکنشهای اکسایش و کاهش، ضروری است. در این مقاله، مفهوم عدد اکسایش، قوانین تعیین آن، کاربردها و نمونه سوالات پرتکرار در امتحانات نهایی و کنکور بررسی میشود.
عدد اکسایش چیست؟
عدد اکسایش (یا حالت اکسایش) عددی است که نشاندهنده توانایی اتم یک عنصر برای از دست دادن یا به دست آوردن الکترون در یک ترکیب شیمیایی است. این عدد به ما کمک میکند تا تغییرات الکترونی در واکنشها را تشخیص دهیم.
به طور کلی:
- عدد اکسایش مثبت نشاندهنده از دست دادن الکترون (اکسایش).
- عدد اکسایش منفی نشاندهنده به دست آوردن الکترون (کاهش).
قوانین تعیین عدد اکسایش
برای تعیین عدد اکسایش عناصر در یک ترکیب، از قوانین زیر پیروی کنید:
- عدد اکسایش عناصر خالص برابر با صفر است.
- مثال: عدد اکسایش O2، N2 و S8 برابر صفر است.
- عدد اکسایش یونهای تکاتمی برابر با بار آنهاست.
- مثال: عدد اکسایش Na+ برابر +1 و Cl- برابر -1 است.
- عدد اکسایش هیدروژن در ترکیبات معمولاً +1 است، مگر در هیدریدهای فلزی که برابر -1 است.
- مثال: در H2O عدد اکسایش هیدروژن +1 و در NaH برابر -1 است.
- عدد اکسایش اکسیژن در ترکیبات معمولاً -2 است، مگر در پراکسیدها که برابر -1 و در فوقاکسیدها که برابر -0.5 است.
- مثال: در H2O عدد اکسایش اکسیژن -2 و در H2O2 برابر -1 است.
- مجموع عددهای اکسایش در یک مولکول خنثی برابر صفر و در یونها برابر بار یون است.
- مثال: در CO2 مجموع اعداد اکسایش صفر است، در H2SO4 مجموع اعداد اکسایش برابر -2 است.
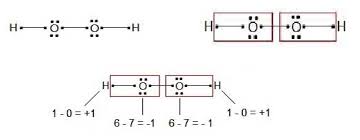
مثالها و محاسبات عدد اکسایش
مثال 1: تعیین عدد اکسایش عناصر در H2SO4
- عدد اکسایش هیدروژن = +1 (با توجه به قانون 3).
- عدد اکسایش اکسیژن = -2 (با توجه به قانون 4).
- مجموع عددهای اکسایش برابر صفر است:
عدد اکسایش گوگرد:
2(+1) + X + 4(-2) = 0
2 + X – 8 = 0
X = +6
بنابراین، عدد اکسایش گوگرد در H2SO4 برابر +6 است.
مثال 2: تعیین عدد اکسایش در -MnO4
- عدد اکسایش اکسیژن = -2 (با توجه به قانون 4).
- مجموع عددهای اکسایش برابر بار یون است:
X + 4(-2) = -1
X – 8 = -1
X = +7
عدد اکسایش منگنز در MnO4- برابر +7 است.
کاربردهای عدد اکسایش
- تشخیص واکنشهای اکسایش و کاهش:
- با مقایسه عدد اکسایش قبل و بعد از واکنش، میتوان مشخص کرد کدام عنصر اکسید شده و کدام کاهش یافته است.
- تعادلسازی واکنشهای ردوکس:
- عدد اکسایش به تعادلسازی دقیق الکترونها در واکنشهای اکسایش و کاهش کمک میکند.
- تحلیل ترکیبات پیچیده:
- عدد اکسایش در درک ساختار و رفتار ترکیبات مانند کمپلکسهای فلزی اهمیت دارد.
سوالات پرتکرار کنکور و نهایی
سوال 1: محاسبه عدد اکسایش
سوال: عدد اکسایش گوگرد در ترکیب SO2 چقدر است؟
پاسخ:
- عدد اکسایش اکسیژن = -2.
- مجموع عددهای اکسایش برابر صفر است:
X + 2(-2) = 0
X – 4 = 0
X = +4
عدد اکسایش گوگرد برابر +4 است.
سوال 2: تعیین تغییرات عدد اکسایش در واکنش زیر:
-2Fe(2+) + Cl2 → 2Fe(3+) + 2Cl
پاسخ:
- Fe: عدد اکسایش از +2 به +3 تغییر کرده است (اکسایش).
- Cl: عدد اکسایش از 0 به -1 تغییر کرده است (کاهش).
سوال 3: تعیین عدد اکسایش در -Cr2O7^2
پاسخ:
- عدد اکسایش اکسیژن = -2.
- مجموع عددهای اکسایش برابر بار یون است:
2X + 7(-2) = -2
2X – 14 = -2
2X = +12
X = +6
عدد اکسایش کروم برابر +6 است.
نکات کلیدی برای موفقیت در مسائل عدد اکسایش
- قوانین عدد اکسایش را حفظ کنید و به ترتیب استفاده کنید.
- برای ترکیبات پیچیده، ابتدا عناصر با عدد اکسایش ثابت (مثل اکسیژن و هیدروژن) را مشخص کنید.
- همیشه مجموع اعداد اکسایش را با بار مولکول یا یون مقایسه کنید.
- سوالات پرتکرار کنکور را تمرین کنید تا در مسائل تسلط پیدا کنید.
جمعبندی
عدد اکسایش یکی از مفاهیم کلیدی شیمی دوازدهم است که در درک واکنشهای شیمیایی و مسائل تعادلسازی واکنشهای ردوکس نقش اساسی دارد. با یادگیری قوانین، تمرین مثالها و حل سوالات کنکور، میتوانید در این مبحث به تسلط کامل برسید.
اگر سوالی دارید، در بخش نظرات بنویسید تا به شما کمک کنیم!